Table of Contents
Obecná chemie
Pojmy
- Avogadrova konstanta - počet částic v 1 molu látky, Na = 6,023 . 10^23 mol^-1
- Molární objem - 22,414 l/mol (při teplotě 273.15 K (bod tání vody) a tlaku 101325 Pa)
- Atomová hmotnostní konstanta je 1/12 klidové hmotnosti atomu uhlíku <m> {}^{12}_{ 6}{C} </m>
- Relativní atomová hmotnost - poměr skutečné hmotnosti atomu k atomové hmotnostní konstantě
Atom
- Protonové (atomové) číslo: počet protonů, Z, dolní index
- Neutronové číslo: počet neutronů, N, u značky prvku se neuvádí
- Nukleonové (hmotnostní) číslo: počet nukleonů, A, horní index, A= Z + N
- Nuklid: množina atomů, mající stejné protonové a neutronové číslo
- Izotop: atomy téhož prvku, které se liší pouze neutronovým číslem
- Radioizotopy : umělé izotopy
- Izobary: Stejné nukleonové číslo, Různé protonové číslo
Radioaktivita
- Radioaktivita neboli radioaktivní rozpad je samovolná přeměna jader nestabilních nuklidů na jiná jádra, při níž vzniká radioaktivní záření, což je ionizující záření vznikající při radioaktivním rozpadu.
- důležitým faktorem stability nuklidu je poměr neutronů N a protonů Z
Jaderné záření
- rozpad nestabilních jader je doprovázen uvolňováním některých částic z prostoru jádra
Záření alfa
- je tvořeno částicemi <m> alpha </m>, což jsou kladně nabitá jádra helia
- má malý dosah, zachytí ho papír, nebo tenké hliníková folie
Záření beta
- je proud záporně nabitých elektronů
- někdy se rozlišuje záření β- (elektrony) a β+ (kladně nabité pozitrony)
- lze ho zachytit 1 cm plexiskla nebo 1 mm olova.
Záření gamma
- je elektromagnetické záření vysoké frekvence, neboli proud velmi energetických fotonů
- nemá elektrický náboj, a proto nereaguje na elektrické pole
- jeho pronikavost je velmi vysoká, pro odstínění se používají velmi tlusté štíty z kovů velké hustoty (např. olovo) a nebo slitin kovů velké hustoty
Radioaktivní rozpady
Rozpad alfa
- z jádra je vymrštěna částice <m> {}^{4}_{ 2}{He} </m>
- rozpadem vzniklý nuklid je v periodické soustavé prvků posunut o dvě místa vlevo oproti původnímu jádru
- A-4, Z-2
Rozpad beta +
- Je emitován elektron.
- Z+1
Rozpad beta -
- Dochází k emisi pozitronu (antičástice k elektronu)
- Z-1
Elektronový záchyt
- Jádro pohltí jeden z elektronů z vnitřních slupek svého obalu a jaderný proton se mění na neutron za současné emise neutrina.
- Elektronový obal je po tomto ději v excitovaném (základním) stavu; místo po zachyceném elektronu nezůstane prázdné, nýbrž je zaplněno elektronem z některého z vyšších atomových orbitalů. Současně dojde k emisi kvanta elektromagnetického záření, tj. fotonu.
- Z-1
Poločas rozpadu
- doba, za kterou dojde k rozpadu poloviny z původního počtu atomů radionuklidu
- <m> T = ln{2}/lambda approx 0,693.lambda^{-1} </m>
Kvantová čísla
- popis elektronů a jejich orbitalů v atomovém obalu
- Hlavní kvantové číslo
- udává energii a příslušnost v jedné ze 7 vrstev (vzdálenost od jádra, velikost orbitalu) – K,L,M,N,O,P,Q, nabývá hodnot 1,2,3,4,5,6,7
- Vedlejší kvantové číslo
- udává tvar orbitalu a také určuje energii e - hodnoty 0 až (n-1), značí se písmeny s,p,d,f
- Magnetické kvantové číslo
- udává vzájemnou polohu orbitalů v prostoru, nabývá hodnot -l ,0,+l, (1 s, 3 p, 5 d a 7 f), všechny orbitaly se stejným m mají stejnou energii, liší se prostorovou orientací = degenerované
- Spinové kvantové číslo
- rotační impuls , nabývá hodnot –1/2 a +1/2
Výstavbový princip
- říká, že orbitaly s nižší energií se zaplňují elektrony dříve než orbitaly s energií vyšší
- v základním stavu atomu tedy elektrony obsazují jednotlivé slupky a podslupky tak, aby měly co nejnižší energii
- orbitaly se tady zaplňují v následujícícm pořadí: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, …
Pauliho princip
- v elektronovém obalu daného atomu může být v konkrétním kvantovém stavu popsaném kvantovými čísly n, l, m, s nejvýše jeden elektron (neboli v daném kvantovém stavu nemohou existovat dva elektrony současně
- každé dva elektrony v obalu se liší v hodnotě alespoň jednoho kvantového čísla
Hundovo pravidlo
- Orbitaly se stejnou energií (= degenerované) se obsazují nejprve po jednom elektronu.
Orbitaly
- typ orbitalu: s, p , d a f
- s - koule, p - osmička, d a f mají složité tvary
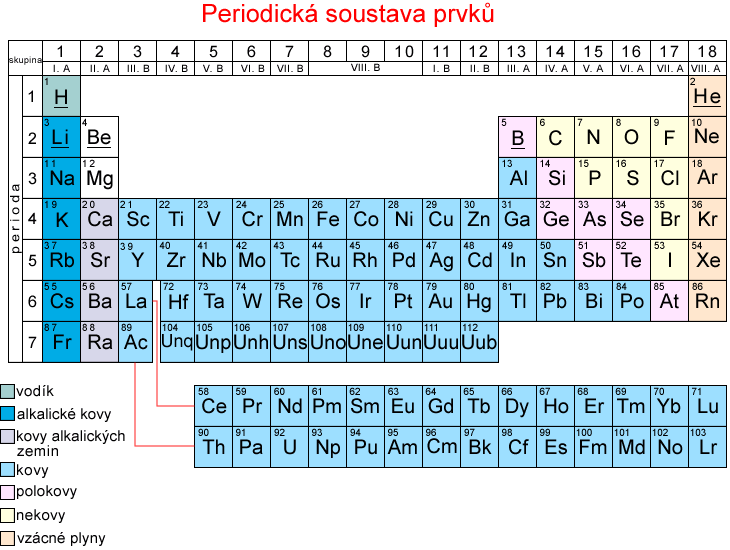
Poloha prvku v periodické soustavě prvků
Periodický zákon
- Vlastnosti prvků se periodicky mění v závislosti na czrůstajícím protonovém čísle.
Periody
- Pořadové číslo periody je totožné s hlavním kvantovým číslem poslední obsazované vrstvy.
Skupiny
- V každé skupině jsou pod sebou seřazeny prvky, které mají stejné počty elektronů v poslední případně předposlední vrstvě el. obalu
- podobné chemické vlastnosti těchto prvků
- poslední vrstva el obalu může obsahovat max 8 el (ns^2np^6)
- zcela zaplněná poslední vrstva je charakteristická vysokou stabilitou
- I – alkalické kovy – Li, Na, K, Rb, Cs, Fr
- II – kovy alkalických zemin – Ca, Sr, Ba, Ra
- III – triely – B. Al, Ga, In, Tl
- IV – tetrely – C, Si, Ge, Sn, Pb
- V – pentely – N, P, As, Sb, Bi
- VI – chalkogeny – O, S, Se, Te, Po
- VII – halogeny – F, Cl, Br, I, At
- VIII – vzácné plyny – He, Ne, Ar, Kr, Xe
Chemická vazba
- spojení mezi atomy, realizované pomocí valenčních elektronů
- atomy prvků (ne vzácné plyny) nemohou trvale samostatně existovat
- Energie chemické vazby: energie, která se uvolní při vzniku chemické vazby
- Disociační energie: energie, potřebná ke zrušení chemické vazby
- Vazba
- jednoduchá (jeden vaz. pár)
- násobná (dva a více vaz. párů)
Vaznost
- udává kolik kovalentních vazeb tvoří prvek v molekule
Excitovaný stav
- Stav energeticky výhodný pro slučování
- Dochází k němu vlivem energie – teplo, světlo:
- Roztržení elektronového páru
- Vypuzení na vyšší orbital
- Tím se např. uhlík stane čtyřvazný
Elektronegativita
- Elektronegativita (Pauling): schopnost vázaného atomu přitahovat elektrony chemické vazby
- rozdíl elektronegativit atomů Δ X: nabývá hodnot od 0 do 4, určuje druh vazby a předpovídá vlastnosti látek
Kovaletní vazba
- mezi stejnými prvky, Δ X = 0
- elektronová hustota rovnoměrně rozložena mezi atomy
Polární vazba
- Δ X = 0,4 - 1,7 …. HCl
- el. pár blíže elektronegativnějšímu prvku (Cl)
Iontová vazba
- Δ X > 1,7 ….. NaCl
- Vpodstatě extrémně polární kovalentní vazba - úplný přesun elektronové dvojice na elektronegativnější prvek
- snadná disociace iontů
- tvorba krystalů
Další typy vazeb
- vazba koordinační
- stejný charakter jako kovalentní, jiný vznik
- celý vazebný pár poskytuje jeden atom (Donor ….. akceptor)
- vazba kovová
- vzniká mezi kovovými prvky ( vlevo a uprostřed periodické tabulky): mají malý počet e v poslední vrstvě a malou elektronegativitu
- má vliv na fyzikální a chemické vlastnosti sloučenin kovů
Van der Waalsovy síly
- jsou přitažlivé nebo odpudivé interakce (síly) mezi molekulami
- nízká energie
- síly columbické, indukční, disperzní
- působení molekulových dipólů (kladné a záporné konce se přitahují)
Vodíkový můstek
- Protože má atom vodíku pouze jeden elektron, dojde při vytvoření vazby k elektronegativnímu prvku ke značnému odhalení atomového jádra. Vzniklý parciální kladný náboj na atomu vodíku může poutat nevazebné elektronové páry okolních molekul (v případě intramolekulární vazby jde o elektronové páry stejné molekuly).
- vzniká když:
- volný e pár na některém z atomů v molekule
- atom H, vázaný s atomem, který má vysokou elektronegativitu, H má kladný náboj
- ovlivňuje fyzikální vlastnosti látek (např. bod varu)
Homogenní a heterogenní směsi
Směsi
- látka, obsahující min. 2 složky, je možné je oddělit fyzikálně-chem. metodami
- Homogenní: má ve všech svých částech stejné vlastnosti (př.: vzduch, roztoky solí), částice < 10-9 m
- Heterogenní: skládá se ze dvou nebo více homogenních oblastí ( fází), (př.: směs práškového zinku a práškové síry)
Dělení roztoků podle skupenství
- Plyny (malá hustota, vyplňují celý prostor, značná tepelná roztažnost, značná stlačitelnost)
- Kapaliny (vyšši hustota, určity objem, prizpusobuji tvar)
- Tuhé látky (objem i tvar, největší hustota, minimální roztažnost a stlačitelnost)
Avogadrův zákon
- Stejné objemy plynů za stejných podmínek (p, T) obsahují stejný počet molekul
Dělení roztoků podle vlastností rozpouštěné látky
- Roztoky neelektrolytů - při rozpouštění látek, jejichž molekuly obsahují nepolární, nebo slabě polární kovaletní vazby
- Roztoky elektrolytů - při rozpouštění iontových sloučenin v polárních rozpouštědlech
Elektolyty
- Silné elektrolyty: alfa → 1 , HCl, HNO3, NaOH, KOH, řada solí
- Slabé elektrolyty: alfa < 0,1 H2S, HCN, organické kyseliny a zásady
- Iontové sloučeniny a sloučeniny s polárními kovalentními vazbami ve vodných roztocích disociují na ionty
- Míra štěpení – disociační stupeň a disociační konstanta (<m> alpha </m>)
- <m> alpha </m> = počet disociovaných molekul/počet všech rozpuštěných molekul
Disociační konstanta
- Vyjadřuje rovnováhu mezi disociovanými a nedisociovanými látkami
- <m> BA right B+ + A-
- <m> K = (B+).(A-)/(BA) </m>
- Velikost pK - rozpoznání slabých a silných elektrolytů
Rozpouštění
- Rozpustnost: hmotnost látky, která se za daných podmínek rozpustí v určitém množství rozpouštědla za vzniku nasyceného roztoku
Rozpouštědla
- Polární – např. voda, methanol: dobře rozpouští látky s iontovou vazbou, dochází k hydrataci volných iontů
- Nepolární – např.chloroform, uhlovodíky: nemísí se s vodou
Látky rozpustné ve vodě
- Oxidy alkalických kovů a kovů alkalických zemin
- Oxidy nekovů mimo SiO2
- Hydroxidy alkalických kovů a kovů alkalických zemin
- Všechny dusičnany, většina síranů a chloridů
- Uhličitany draslíku a sodíku
Nerozpustné
- Oxidy ostatní
- Hydroxidy ostatní
- Dusičnan Bi
- Sírany Ba, Sr, Ca, Ag, Ra
- Chloridy Ag, Pb, Hg
- Většina uhličitanů a fosforečnanů
Chemické reakce
dělení podle vnějších změn
- skladné - syntézy (jednodušší molekuly → složitější molekuly)
- <m> 2H_2 + O_2 right 2H_2O </m>
- rozkladné (složitější molekuly → jednodušší molekuly)
- <m> CaCO_3 right CaO + CO_2 </m>
- substituční - vytěsňovací (jedna skupina nahradí jinou)
- <m> Zn + CuSO_4 right ZnSO_4 + Cu </m>
- konverze - podvojná záměna ( výměna skupin)
- neutralizace <m> NaOH + HCl right NaCl + H_2O </m>
- srážecí reakce
rozdělení podle skupenství reaktantů
- Reakce homogenní plyn + plyn → plyn
- Reakce heterogenní plyn + kapalina → kapalina
rozdělení podle přenášených částic
- Reakce acidobazické: kyselina + zásada → sůl
- Reakce oxidačně-redukční: přenos elektronů mezi reagujícími látkami (změna oxidačních čísel některých atomů)
- Komplexotvorné: tvorba koordinačně kovalentní vazby
rozdělení podle tepelného zabarvení
- exotermní - teplo se uvolňuje
- andotermní - teplo se spotřebovává
Roztoky
- Kyselé, zásadité, neutrální
- Koncentrace OH- nebo H_3O+
- Neutrální roztok: molární konc. OH- nebo H3O+ je stejná
- Kyselé roztoky: molární koncentrace H3O+ je větší než 1,0.10-7 mol/l
- Zásadité roztoky: molární koncentrace H3O+ je menší než 1,0.10-7 mol/l
- konstanta acidity <m>K_A = ([H_3O^+].[B^- ])/([HB])</m>
- konstanta bazicity <m>K_B = ([Z^+].[OH^- ])/([ZOH])</m>
- pH - koncentrace oxoniových kationtů
- pOH - koncentrace hydroxidových aniontů
- pH + pOH = 14
- Kyselé roztoky: pH < 7
- Zásadité roztoky: pH > 7
- Kyselina: látka, schopná ve vodných roztocích odštěpovat vodíkový kation H+, odštěpující proton (donor protonů)
- Zásada: látka, schopná ve vodných roztocích poskytovat anion OH-, schopná přijmou proton (akceptor protonů)
- Protolytická reakce: dochází k výměně protonů nebo H+
- Protolyt: kyseliny a zásady
- Amfolyt: chová se jako kyselina i zásada
Neutralizace
- v roztoku kyseliny H+, v roztoku zásady OH-
- vzájemnou reakcí H+ a OH- vzniká voda, reakci kaniontu kovu s aniontem kyseliny vzniká sůl
<m>H^+ + OH^- → H_2O</m>
<m>K^+ + Cl^- → KCl</m>
Hydrolýza
- Protolytická reakce solí s vodou
- Dochází k posunu pH
- Silná kyselina + slabá zásada → kyselý roztok
- Slabá kyselina + silná zásada → zásaditý roztok
- Silná kyselina + silná zásada → neutrální roztok
- Ovlivnění teplotou a ředěním
Oxidace a redukce
- oxidace je děj při kterém se zvyšuje oxidační číslo
- redukce je děj při kterém se snižujeoxidační číslo
Oxidační číslo
- náboj, který by byl přítomen na atomu prvku, kdybychom elektrony všech vazeb přidělili vždy elektronegativnějšímu atomu
Oxidační činidlo
- látka, která dokáže jiné lárce odebrat elektrony a tím ji oxidovat
Redukční činidlo
- dodává do systému elektrony, čímž se redukuje
Chemická termodynamika
Soustava
- otevřená
- uzavřená
Termochemie
- zabývá se studijem tepelného zabarvení chem. reakcí
- Standardní stav = takový stav látky, ve kterém je při teplotě 168,15 K a tlaku 101,325kPa látka nejstálejší.
- exotermní děj <m> - Delta H </m>
- endotermní děj <m> Delta H </m>
Termochemické zákony
1. termochemický zákon (Laplaceův-Lavoisierův)
- Hodnota reakčního tepla přímé nebo protisměrné reakce je stejná, mění se však hodnota jeho znaménka (+/-).
2. termochemický zákon (Hessův)
- Výsledná hodnota reakčního tepla nezáleží na průběhu chemické reakce, ale pouze na jeho počátečním a konečném stavu.
Standardní slučovací teplo
- Teplo, při kterém vzniká 1 mol látky přímo z prvků, reakční látky musí být ve standardním stavu. Standardní slučovací tepla prvků jsou rovna nule.
Standardní spalné teplo
- Teplo, při kterém se spálí 1 mol látky v nadbytku kyslíku.
Teorie aktivních srážek
- nutná srážka mezi reag. molekulami
- částice musí mít dostatečnou energii
- částice musí mít vhodnou prostorovou orientaci
- minimální účinná energie aktivační
- aktivační energie = součtu energií všech zanikajících vazeb